脊柱外科手术,您循证了吗?
2017-08-31 文章来源:首都医科大学附属北京朝阳医院 潘爱星 海涌 点击量:1414 我要说
脊柱疾病的复杂性和多变性决定了脊柱外科医生会不断面对新的挑战。同种疾病的治疗方法和理念会随患者所处的不同历史时期而不断变化。随着医学科技的快速进步和医学经验的不断积累,历史上许多被称为“经典”的治疗手段已被尘封。即使在当下,脊柱外科领域对疾病的诊疗观念仍存在不断的争议和激烈的碰撞。
争议之所以存在,其原因是缺乏足够有说服力的证据。前瞻性随机对照研究能给我们最高等级的证据支持,在争议中寻找最合理的答案,而往往这类高级别证据如凤毛麟角,不可多得。当然,争议才是学术生命力的象征,是科学发展进步的根本动力。
本文结合近期发表在脊柱外科顶级学术期刊Spine上的系统回顾文章“Evidence-based Recommendationsfor Spine Surgery“, 给大家盘点脊柱外科领域6个颇具争议的话题。正所谓:他山之石,可以攻玉,希望本文能给脊柱外科同道们带来帮助。

该文由美国著名脊柱外科专家AlexanderVaccaro教授执笔,通过对近几年脊柱外科领域相关热点问题的几个著名研究报告论文进行详细分析评价,以期对这些焦点热点问题有一个初步的循证共识。
1、腰椎退变性滑脱合并腰椎管狭窄症——减压后需要融合吗?
目前,对于腰椎退变性滑脱合并腰椎管狭窄症减压后是否需要植入椎弓根螺钉内固定进行融合在文献中仍存在争议。前瞻性非随机对照研究表明,相比与单纯减压,融合能够给患者带来更好的临床疗效;但也有5年随访的前瞻性研究表明单纯减压亦能够获得良好的疗效。以往研究受限于证据等级不足仍未能给出最终的答案。

Ghogawala等进行了单纯减压与减压后融合治疗退变性腰椎滑脱合并腰椎管狭窄症的随机对照研究,研究成果于2016年发表在New England Journal of Medicine杂志(Ghogawala Z, Dziura J, Butler WE, et al. Laminectomy plus fusionversus laminectomy alone for lumbar spondylolisthesis. New Engl J Med2016;374:1424–34)。研究纳入患者66名,其中35名进行单纯减压术,31名进行减压融合术。两组完成2年随访的患者数分别为29名和28名。
在2年随访时,单纯减压组患者SF-36评分改善值为9.5,融合组为15.2,二组相差5.7,差异有统计学意义(P=0.046)。除了在术后1年随访点时SF-36改善值差异无统计学意义,在术后3月、6月、和4年时,融合组的改善情况均优于单纯减压组。然而,在ODI评分的改善方面二组患者在各个时间点的改善差异均无统计学意义。同时,融合组手术并发症发生率显著较高(失血量、住院时间、手术时间),但是再手术率更低(14% vs. 34%)。
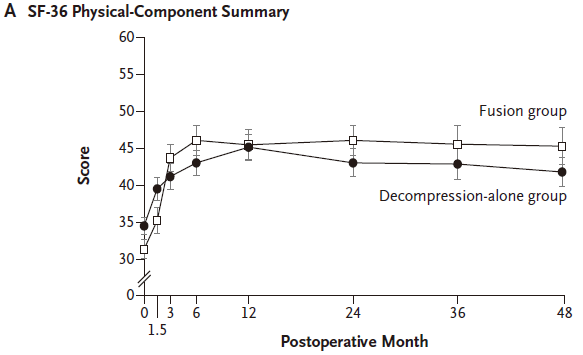
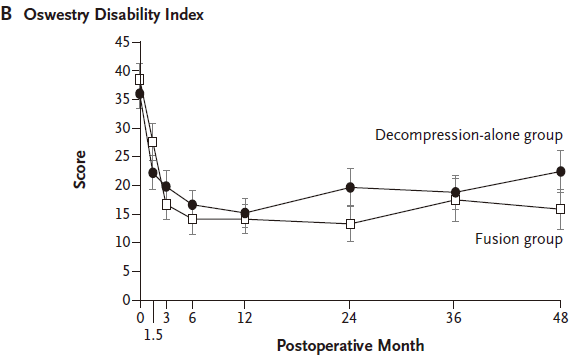

研究结论:对于退变性腰椎滑脱合并腰椎管狭窄症患者,减压融合术在术后4年能够给患者带来更好的临床效果和生理功能的提高。同时,作者认为虽然两组患者ODI评分改善没有表现出差异,但ODI评分主要针对于下腰痛导致的功能障碍评估,而对于腰椎滑脱合并腰椎管狭窄症患者往往更重要的是解除神经源性间歇性跛行,SF-36对于这类患者术后生理功能改善的评估更加适用。
(Recommendation:强烈推荐)
2、腰椎管狭窄症——单纯减压可以吗?
那么,对于腰椎管狭窄症患者,减压后是否需要融合呢?Forsth等进行了一项单纯减压与减压融合术治疗的随机对照研究,研究成果发表在NewEngland Journal of Medicine杂志2016年374卷15期(Forsth P,Olafsson G, Carlsson T, et al. A randomized, controlled rial of fusion surgeryfor lumbar spinal stenosis. New Engl J Med 016;374:1413–23)。

研究中纳入247名患者,其中123名分配至单纯减压组,124名分配至减压融合组。患者的纳入标准为:年龄50-80岁;神经源性间歇性跛行病程大于6个月;VAS评分大于30(100);1-2个节段狭窄,硬膜横截面积小于等于75mm2;有/无腰椎滑脱,滑脱标准为侧位X线片椎体滑移大于等于3mm。最终完成手术并随访的患者共228名。
减压融合组手术时间、术中出血量、住院时间(7.4天 vs. 4.1天)、患者花费($12,000 vs. $5,400)显著高于单纯减压组。但是二组患者围手术期并发症和再手术率无显著差异。术后2年随访时,二组患者主要评估指标ODI评分改善情况差异无统计学意义,亚组分析结果表明滑脱组与非滑脱组的改善情况也一致。
与此同时,次要评估指标:欧洲五维生活质量量表, VAS-腰痛, VAS-腿痛, Zurich间歇性跛行问卷评分, 6分钟行走测试和患者满意度调查的改善情况二组均无差异。228名患者中144名完成5年随访,5年随访结果同上。
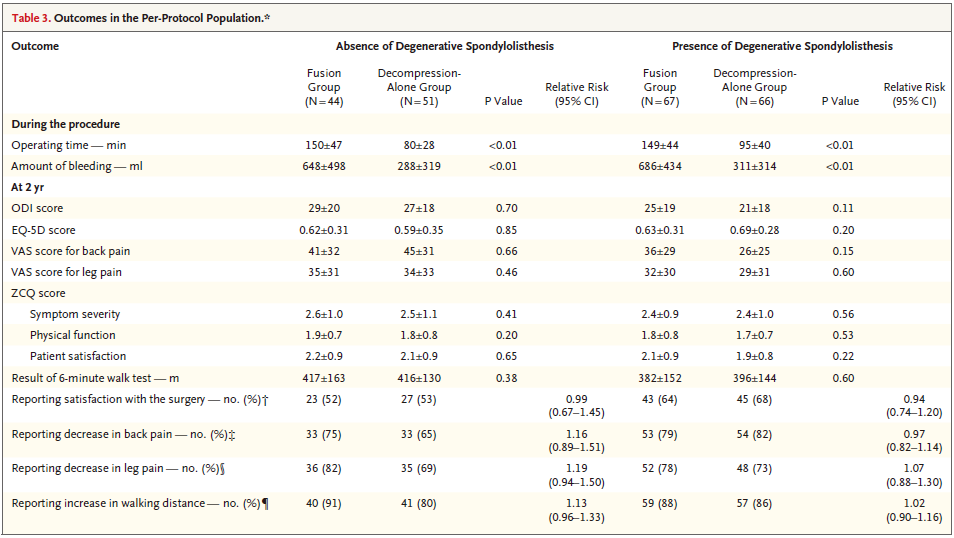
研究结论:对于腰椎管狭窄症患者,额外的融合并不能给患者带来更好的临床收获,反而增加了术中出血量、延长了患者住院时间、增加了患者直接花费。不仅如此,作者认为,即使存在腰椎滑脱,融合也没有提高临床疗效,降低再手术率。
(受手术减压方式有差异等方法学限制,Recommendation:弱推荐,尤其对腰椎管狭窄症合并腰椎滑脱的患者)。
3、如何判断脊髓型颈椎病(Cervical Spondylotic Myelopathy, CSM)患者的手术预后?
要准确地判断CSM患者的手术预后目前仍然是个难题。正确地判断手术预后有助于患者对治疗预期的设定和医生治疗决策的制定。为此,全球最大的脊柱外科学术组织AOSpine进行了一项多中心研究,旨在建立CSM患者手术预后的预测模型(Tetreault LA, Kopjar B, Vaccaro A, et al. A clinical predictionmodel to determine outcomes in patients with cervical spondylotic myelopathyundergoing surgical treatment: Data from the prospective, multi-center AOSpineNorth America study. J Bone Joint Surg Am 2013;95:1659–66)。

研究中278名患者来自北美CSM研究学组,479名患者来自国际CSM研究学组(16个国家),共757名。其中14名患者术前JOA评分较低而被排除,614名患者完成1年随访。743名患者中,193名轻度CSM,196名中度CSM,354名重度CSM。该研究虽然未能制定手术预后的预测模型,但研究表明影响CSM患者术后JOA改善的因素有:术前JOA评分、受损步态、高龄、伴随疾病、吸烟和病程。

(Recommendation:弱推荐)
4、腰椎间盘突出髓核切除术后再手术率几何?
腰椎间盘突出症行髓核切除后再手术率在众多研究中变异较大。Leven等进行的大样本长期随访研究给了我们较为可信的答案(Leven D,Passias PG, Errico TJ, et al. Risk factors for reoperation in patients treatedsurgically for intervertebral disc herniation: A subanalysis of eight-yearSPORT data. J Bone Joint Surg Am 2015;97:1316–25)。

该研究共纳入810名术后随访至少8年的患者。患者手术节段57%为L5/S1,39%为L4/5,3%为L3/4,2%为L2/3。119名(15%)患者术后8年内行再手术。其中因椎间盘突出复发行再手术的患者占62%(86%为原手术节段,11%为其它手术节段,3%未知),因手术并发症再手术者占25%,因新发临床症状行再手术者占11%。再手术主要发生在术后2年内,因椎间盘突出复发而再手术的风险随着时间延长而降低:第一年下降4%,此后每年平均下降0.5%-1%。因各种原因的再手术率亦随时间延长而下降:第一年下降6%,第二年下降2%,此后每年平均下降1%。

腰椎间盘突出的节段和类型并没有影响再手术的发生率,影响术后再手术率的因素为:年龄(行再手术的患者普遍较年轻)和不对称的肌肉无力(肌力下降的患者再手术率低,文中并未对这一不寻常的现象进行分析)。此外,再手术组患者平均住院时间较长,术后感染率较高,术后并发症发生率较高。其它因素,如:吸烟、糖尿病、肥胖、抑郁、工作收入和工作提升的需求并未对再手术的发生率产生影响。当然,行再手术的患者的满意度和临床疗效评估均较差。
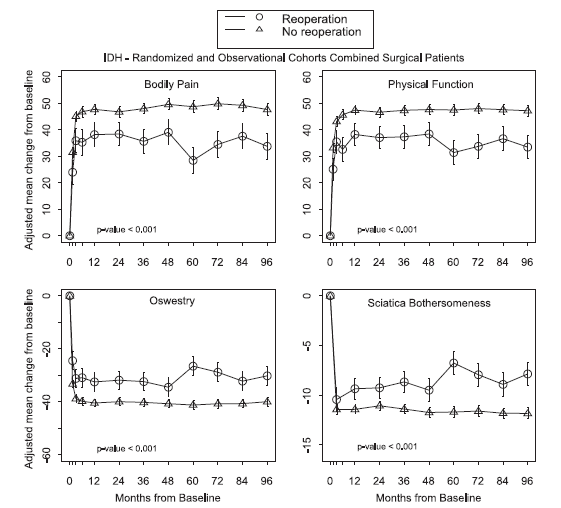
(Recommendation:不需要改变目前临床实践)
5、胸腰椎骨折——保守与手术治疗对椎间盘退变的影响
脊柱内固定术能够稳定脊柱、矫正畸形,因此是治疗脊柱骨折最常用的方式。但固定融合术后邻近节段应力增加导致继发的邻近节段退变(adjacent segment degeneration, ASD)仍然是临床医生不得不面对的问题。ASD是脊柱内固定后生物力学改变导致的还是正常自然退变过程?众说纷纭。

为了比较无椎间盘退变疾病患者发生胸腰椎骨折后行内固定手术治疗与保守治疗后椎间盘退变发生率和因椎间盘退变而再手术率的不同,D'Oro等回顾分析了美国骨科医疗系统诊断为胸椎/腰椎骨折的患者(D’Oro A, Spoonamore MJ, Cohen JR, et al. Effects of fusion andconservative treatment on disc degeneration and rate of subsequent surgeryafter thoracolumbar fracture. J Neurosurg Spine 2016;24:476–82)。其中胸椎骨折3699名,腰椎骨折5016名。胸椎骨折患者中117名(3.2%)行融合手术治疗,3215名(86.9%)行非手术治疗。
随访3年后,非手术组中147名(4.6%)患者发生胸椎间盘退变疾病,11名患者因此行手术治疗;融合组1-11名(0.9%-8.5%)(因患者隐私保护的原因,作者无法确定具体人数)患者发生胸椎间盘退变疾病,因此行二次手术的患者为0%。二组胸椎间盘退变的发生率差异无统计学意义(P>0.05)。腰椎骨折患者中,4371名(87.1%)患者行非手术治疗,150名(3.0%)患者行融合手术治疗。随访3年后,融合手术组患者腰椎间盘退变疾病的发生率显著高于非手术治疗组(23.3% vs.11.5%,P<0.05),二组之间因腰椎间盘退变再手术比率无显著差异。
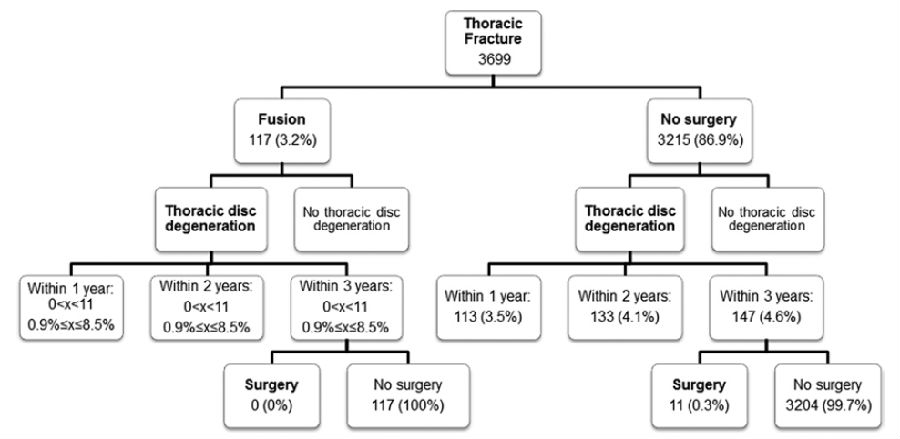
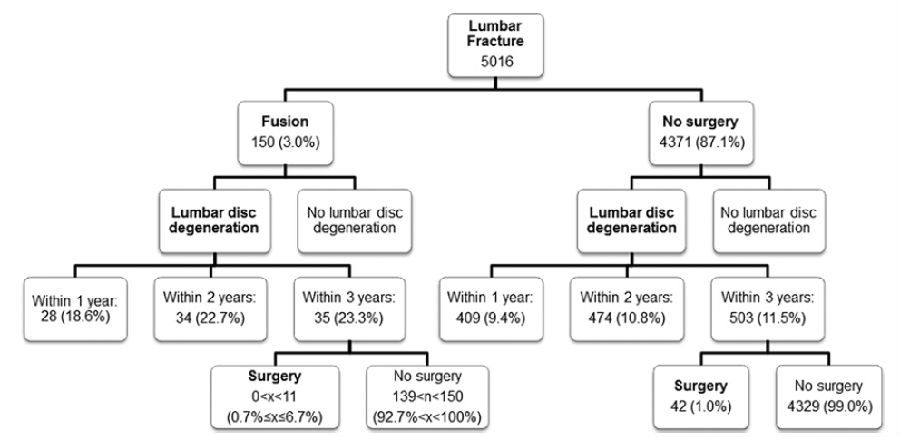
研究结论:胸椎骨折行内固定融合术不会增加胸椎间盘退变疾病的发生率和再手术率,但是腰椎骨折行内固定术后腰椎间盘退变疾病的发生率则显著升高。
(由于研究设计缺陷和不可控的偏倚较多,Recommendation:不需要改变目前临床实践)
6、成人脊柱畸形矫形手术——神经安全知多少?
随着手术技术的提高,成人脊柱畸形(adult spinal deformity, ASD)患者行手术治疗的越来越多。由于ASD患者脊柱畸形和和伴随疾病的复杂性,手术治疗的并发症发生率较高,尤其是神经相关并发症。由于缺乏高等级临床研究,目前仍无法对ASD矫形手术神经功能的安全性和有效性下定论。

Lenke教授进行了一项前瞻性、国际多中心研究(Lenke LG, Fehlings MG, Shaffrey CI, et al. Neurologic outcomes ofcomplex adult deformity surgery. Results of the prospective, multicenterScoli-RISK-1 study. Spine 2016;41:204–12),为探究ASD术后神经功能的预后。
研究共纳入272名ASD患者,来自5个国际脊柱中心(43名脊柱外科医生),所有患者随访时间至少1年。患者均诊断为:复杂ASD,顶椎位于C7-L2,主弯Cobb角≥80°。主要评估方法为ASIA下肢肌力评估量表(American Spinal Injury Association Lower Extremity Motor Score, ASIA LEMS)(评估对象:髂腰肌、股四头肌、胫前肌、伸姆长肌和腓肠肌),每块肌肉0-5分,共50分(双侧)。所有患者术前6周、住院时、术后6周和术后6个月分别进行ASIA评估,评估结果分类为:无变化,改善和加重。
术前神经功能正常者204例,异常者68例。LEMS评分在住院时较术前6周有22.18%患者下降,12.78%患者上升;术后6周较住院时17.9%患者下降,16.42%患者上升;术后6月10.82%患者神经症状加重,20.52%患者改善,68.66%患者无变化。总体上,术前神经功能正常组患者术后LEMS评分下降,但是术后神经功能异常在术后6月随访时均有显著改善。
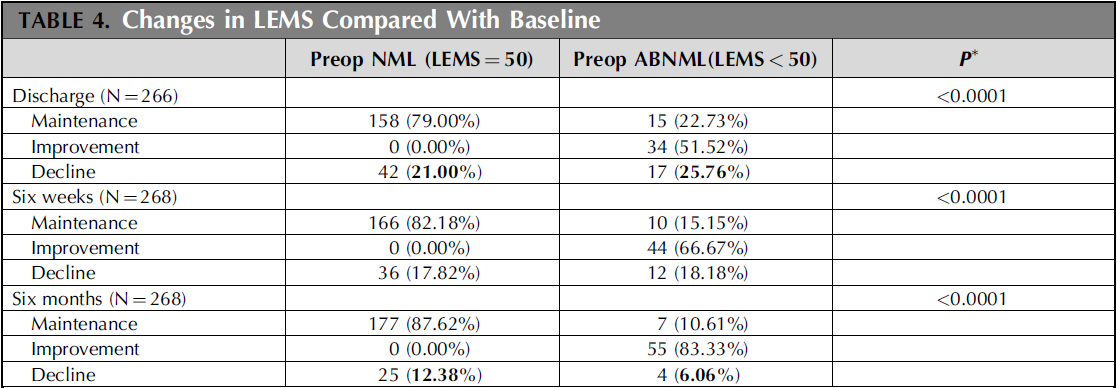
研究结论:复杂成人脊柱畸形矫形手术后神经功能异常发生率远较既往报道的20%要高。但是,大多数术后神经功能异常表现为一过性,患者的肌力能在术后6月内获得恢复。
(Recommendation:不需要改变目前临床实践)
随着老年化社会的到来,脊柱疾患有效安全的手术治疗是提高疗效、减少损害的关键。尽管循证医学的证据可以为大家提供有益的参考,但作为脊柱外科医生,在循证医学证据的基础上对每一位患者选择个体化的精准手术治疗手段,才是我们在日常临床实践中需要时刻关注的。




 京公网安备11010502051256号
京公网安备11010502051256号