“龙门吊”——严重胸椎黄韧带骨化症外科治疗的新方法
2018-08-22 文章来源:海军军医大学附属长征医院 作者:孙凯强 孙璟川 史建刚 点击量:2737 我要说
编者按
胸椎黄韧带骨化是造成胸椎管狭窄的主要原因之一。椎板切开术和椎板切除术是胸椎黄韧带骨化患者主要的治疗手段,然而对于严重的胸椎黄韧带骨化患者,传统治疗方法的临床疗效仍存在争议。其中,脑脊液漏,脊髓损伤,和急性神经功能恶化等并发症的发生已经成为黄韧带骨化外科治疗的难题。
海军军医大学附属长征医院史建刚教授认为,脊髓的减压应该以恢复脊髓原始生理环境为目的,传统的椎板切开或椎板切除均增大了脊髓后侧的空间,这虽然在一定程度上实现了减压,但是脊髓的原始生理环境遭到改变,可能导致脊髓后方漂移而产生生理状态的变化,造成不利于病人神经功能完全恢复。
基于“脊髓原位减压”理论,史建刚教授在提出ACAF手术治疗颈椎后纵韧带骨化后,再次创新性提出“龙门吊”脊髓原位减压术治疗胸椎严重后纵韧带骨化。
什么是胸椎黄韧带骨化?
1920年Polar教授通过X线第一次诊断并命名了胸椎黄韧带,之后,胸椎黄韧带逐渐成为胸椎脊髓压迫的主要原因之一[1]。同后纵韧带骨化一样,胸椎黄韧带骨化主要发生在亚洲人群。据报道,日本整体发病率约36%,亚洲南部地区发病率为3.8%[2-4]。从解剖学角度看,胸椎黄韧带主要由内侧的椎板部分和两侧的囊部分组成。通常情况下骨化开始形成于囊部分,然后逐渐向中间和腹侧发展。最后双边骨化的黄韧带在椎板中部融合增厚形成巨大块状骨化物。因此根据CT上骨化黄韧带发展的过程,Sato T等将骨化黄韧带分为五种类型[5](图1):
1.侧块型:骨化仅局限于黄韧带囊性部分;
2.延伸性:骨化向韧带中间部发展,但仍然较薄;
3.扩大型:骨化物宽度与延伸型相似,但是厚度增加,造成椎管后正中部狭窄;
4.融合型:骨化位置类似扩大型,但是双边骨化病变在中部融合;
5.结节型:双边骨化块在中间融合增厚,呈结节状凸向椎管。
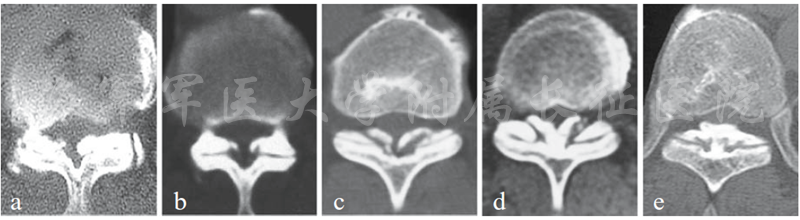
图1胸椎黄韧带骨化的影像学分型 a 侧块型;b 延伸型;c 扩大型;d 融合型;e 结节型 (摘自《Ossification of posterior longitudinal ligament》,第二版, K. Yonenobu;K. Nakamara等)
传统胸椎黄韧带骨化的治疗[5]
由于黄韧带骨化起病隐匿,所以等到病人有症状时,大部分都已经需要手术治疗。胸椎黄韧带骨化的手术治疗基于黄韧带发展的过程。French-door椎板切开术适用于侧块型,延展型和扩大型的黄韧带骨化。该手术先在目标椎板最上方和最下方做两横行切口,通过在椎板中间的纵型切口和双侧或单侧的纵型切口完成“门”的制作,最后从中线处打开椎板完成椎管扩大减压。En bloc椎板切除术适用于融合型和结节型黄韧带骨化。由于骨化物跨过椎板中间部,中线切口操作将存在困难,因此椎板切除术通过上下方两横切口和双侧两纵切口完成病变椎板的游离,最后通过移除椎板完成椎管扩大减压。
椎板切开术简单但是适应症有限,对于严重压迫的黄韧带骨化减压效果欠佳。椎板切除术减压充分,但是对术者手术水平要求较高。同时由于严重的黄韧带骨化常常合并硬膜囊骨化,脑脊液漏和脊髓损伤的发生率较高。
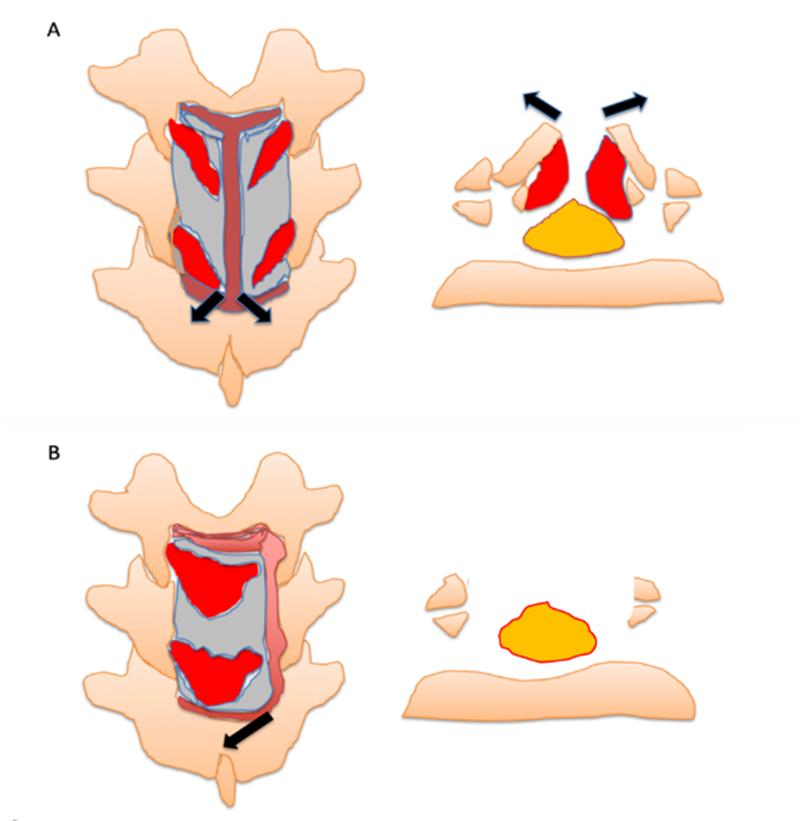
图2 治疗黄韧带骨化传统治疗方法:A French-door椎板开术;B:En Bloc椎板切除术
黄韧带骨化治疗新方法——“龙门吊”脊髓原位减压术
1.麻醉、病人体位和暴露
病人在气管麻醉之后,呈俯卧位。术中影像学检查确定好手术水平后,与背部正中做一纵型切口,分离皮下组织,逐步暴露棘突,双侧椎板和横突(图3A, 4A)。
2.椎板-骨化物复合体游离,安装龙门吊桥
椎板-骨化物复合体分离类似椎板切除术椎板的游离。黄韧带通常不存在于椎弓根的内侧缘,因此沿椎弓根内侧缘做纵型切口可以避免损伤黄韧带(图3B)。术中两种形切口在骨化物外侧缘与椎弓根内侧缘之间,宽度约2mm。切除手术节段范围内的棘突,保留棘突的基底部,随后使用巾钳在棘突基底部两侧约5mm作一骨性通道(10mm宽,5mm深),同时贯穿预留一胸科缝线以利于后面的“吊起”操作(图3C,4C)。然后在手术节段下方椎弓根水平作横切口连接双侧纵切口(图3D)。随后在双侧相应位点植入椎弓根钉,纵型钛棒和横型钛棒,完成“吊桥”的安装(图3E,4D)。将胸科缝线打一滑结,使得椎板-骨化黄韧带复合物暂时固定(图3F,4E)。最后在手术节段最下方作第二个横切口,完成复合物的完全游离(图3G)。
3.椎板-骨化黄韧带复合物的提拉
在完全游离复合物后,逐渐收紧胸科缝线使得复合物逐渐向后方移动。在操作过程中,可看到复合物随着硬膜会发生同节律的搏动,这提示脊髓逐渐获得了减压。复合物向后方提拉的距离由术前骨化物的厚度决定。在提拉过程中,通过调整横行钛棒的弯曲度和椎弓根钉植入的深度可以进一步增加提拉的距离。提拉完成后通过进一步打外科结使得复合物固定在“吊桥”上(图4F)。最后,使用咬碎的棘突骨完成双侧纵形切口和横行切口的填补融合。整个手术过程中,需要检测患者的神经电生理指标,包括体感诱发电位和运动诱发电位。
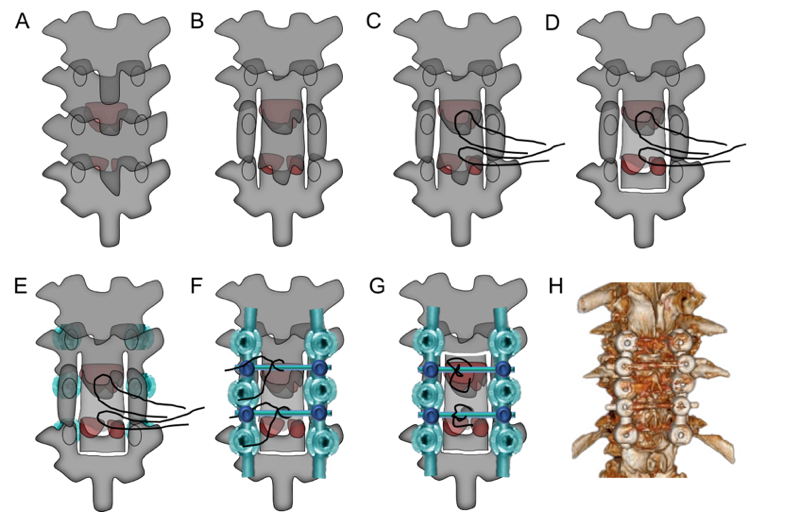
图3 “龙门吊”脊髓原位减压术前后位示意图
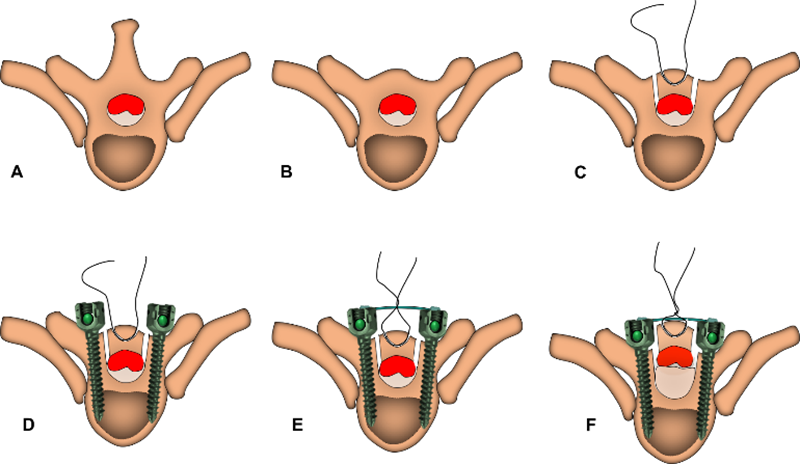
图4 “龙门吊”脊髓原位减压术横断位示意图
4.病例展示
58岁女性患者,由于双下肢麻木、疼痛和行走障碍伴小便障碍两年,加重一月来我院就诊。术前X线片提示在T9/10h和T10/11处存在高密度影。进一步CT检查确诊为该节段黄韧带骨化,呈结节型和扩大型压迫脊髓,最高脊髓侵占率达71.61%(图5)。

图5 病人术前影像学资料
在完善进一步检查后为该病人实施“龙门吊”脊髓后方减压术。整个手术过程分为病人术前准备,术中暴露,复合物游离,“吊桥”安装和最后的提拉。图6是术中的实际操作图和示意图。整个手术过程,病人电生理状态良好。
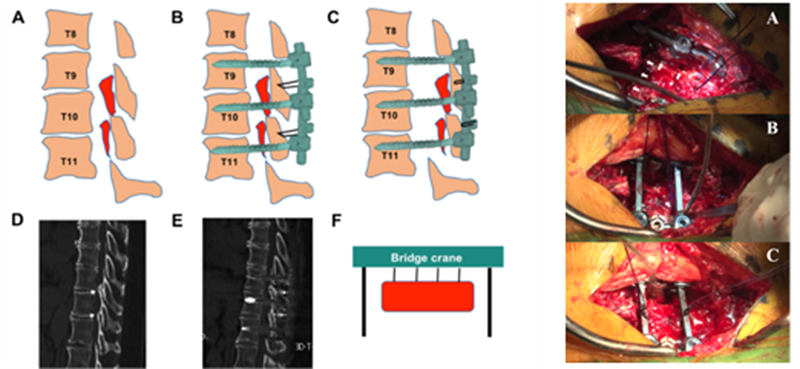
图6 该病人手术示意图和术中操作图
在术后6个月的随访中,病人未出现手术相关的的并发症。病人的肌力由术前的1恢复到最后随访的4.下肢运动和感觉障碍也得到了明显的恢复,病人可以不需要辅助独立行走。病人的泌尿系统功能也得到了明显的改善。JOA评分恢复率在随访的3月和6月分别为50%和75%。术后影显示脊髓获得了充分的减压,脑脊液带也获得了满意的恢复。在最后的随访中,X线提示“吊桥”位置良好,患者植骨也得到了很好的融合。
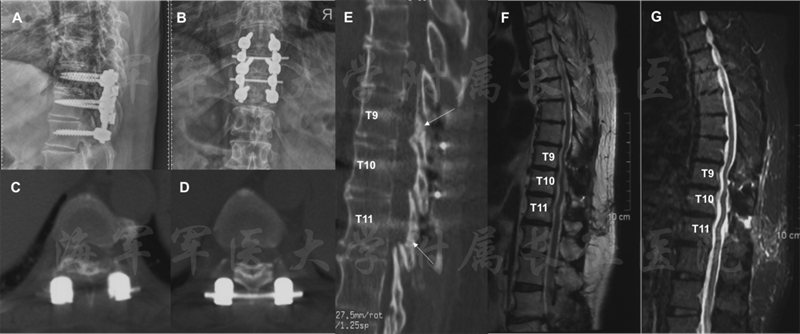
图7 患者术后6月随访影像学资料
5.胸椎黄韧带骨化治疗新思路
黄韧带骨化常常发生在下位胸椎,T9-12最多见。病人早期多表现为麻木和轻微的感觉异常,常常被忽视。一旦症状加重,多提示脊髓受压已经非常严重,往往需要手术治疗[6,7]。传统的减压主要包括椎板切开术和椎板切除术。如上所述,两类手术方式均在一定程度上实现了脊髓的减压,但是仍存在特有的并发症,限制了其在临床上广泛的应用。如本文展示病例,由于病人的骨化的黄韧带已经跨过椎板中线,所以椎板切开术不适用。而椎板切除术由于其需要切除骨化物,所以对于合并硬膜囊骨化的病人,其硬膜囊撕裂和脑脊液漏的发生率也较高[8,9]。
“龙门吊”脊髓原位减压术的核心操作就是完成椎板-骨化黄韧带复合物的游离,通过复合物整体向后方提拉完成脊髓的局部减压,这与史建刚教授同时提出的ACAF治疗颈椎后纵韧带骨化的核心理念一致,都遵循“脊髓的原位减压”理论[10]。通过术前确定合适的提拉距离,术中合理调整椎弓根钉长度和植入深度以及横行钛棒预弯的曲度,实现脊髓的充分减压。
同时对于黄韧带骨化合并硬膜囊骨化问题,一直是传统手术经常遇到的难题。Miyakoshi等曾报道在融合型和结节型黄韧带骨化的病人中,硬膜囊骨化或粘连的发生率高达56%[11]。这种情况下,对于骨化粘连硬膜囊的处理将增加手术的操作,如对于撕裂硬膜囊的修补,也有学者提出不完全切除骨化黄韧带,而是使用漂浮方法完成减压,但是该术式的减压效果仍然存在争议[12,13]。“龙门吊”脊髓原位减压术通过完整提拉复合物可以很好的避免了直接对于骨化物进行分离、切除等操作,很大程度上降低了硬膜囊撕裂和脑脊液漏的发生率。
急性神经功能恶化是椎板切除术较为少见的并发症。Young等曾报道胸椎管狭窄病人神经功能恶化发生率为14.5%,远远高于颈椎管狭窄病人(0-5.5%)[14]。从解剖学角度,胸椎椎管容积相对较小,血供相对脊髓其他区域也较少。Takai等认为黄韧带骨化造成胸椎管狭窄后,会有血管代偿长入骨化组织和脊髓,而切除骨化物后,破坏静脉引流将造成局部脊髓血液循环障碍,引起神经功能恶化[15,16]。在“龙门吊”脊髓减压过程中,骨化组织得以保留,可以避免相关血管的损伤。同时对于复合物的提拉是逐渐的可控的,可以一定程度上降低突然的血液灌注造成的脊髓损伤。
“龙门吊”脊髓原位减压术实现脊髓减压的同时最大程度保留了胸椎结构的完整性。根据长征医院脊柱二科的临床经验,我们认为该术式对于胸椎黄韧带骨化的病人是相对安全和有效的。我们未来还会对该术式进行进一步深入研究,随访更多的病例来评估该术式对于胸椎黄韧带骨化的手术疗效。
作者简介

孙凯强
海军军医大学附属长征医院脊柱二科 硕士研究生
研究方向:脊柱脊髓发育畸形的发病机制、椎间盘退变

孙璟川
上海长征医院骨科医院脊柱二科,讲师、主治医师。
2015年前往美国学习脊柱微创技术和脊柱外科机器人技术。主要研究方向为精准脊柱外科技术,参与设计和实施了包括脊髓栓系综合征Capsule手术、骨折疏松性压缩性骨折Nice手术及颈椎后纵韧带骨化症ACAF手术等创新技术。目前共撰写获得AOSpine国际基金1项、国家课题1项及上海市课题2项。在专业顶级期刊发表SCI论文15篇,主编英文专著1部,副主编专著2部,参编4部。获批发明专利6项,实用新型专利3项。中国医药教育协会骨科专业委员会脊柱分会青年委员;中国医药教育协会骨科专业委员会脊柱分会颈椎学组委员;中国康复辅助器具协会肢体功能重建与外固定委员会委员;北美脊柱外科协会国际会员。

史建刚
主任医师,教授
博士及硕士研究生导师
上海市领军人才
上海市“新百人”
海军军医大学附属长征医院骨科医院脊柱二科主任
学术创新:
提出了脊髓原位减压的理论,发明了严重后纵韧带骨化病前路外科治疗的ACAF技术
发明腰椎脊髓栓系综合征capsule手术技术
发明胸腰椎骨质疏松性骨折NICE微创技术
提出脊髓栓系综合征“脊柱脊髓发育不匹配”理论
提出“腰骶神经弓弦病”概念及理论
学术专长:
颈椎病、腰椎病的外科治疗及微创治疗
重度颈椎后纵韧带骨化症
脊柱脊髓发育性畸形(脊髓拴系综合征、半椎体畸形、颈椎畸形等)
腰骶神经弓弦疾病
学术任职:
中华医学会骨科学分会脊柱学组 委员
中国康复医学会脊柱脊髓专业委员会 委员
中国医师协会骨科分会脊柱专家组 委员
中国人民解放军骨科专业委员会及脊柱学组 委员
中国医药教育协会骨科专业委员会 副主任委员
中国医药教育协会骨科专业委员会脊柱分会 主任委员
《Spine Journal》英文版 编委
《Asian Spine Journal》英文版 编委
主要荣誉:
发表文章50余篇,SCI40余篇
主编专著6部,在编3部
获国家、军队及省部级课题10余项
获国家、军队及省部级奖项10余项
获国家发明及实用新型专利30余项
立三等功2次
参考文献
[1] Hou X, Sun C, Liu X, Liu Z, Qi Q, Guo Z, Li W, Zeng Y, Chen Z (2016) Clinical Features of Thoracic Spinal Stenosis-associated Myelopathy: A Retrospective Analysis of 427 Cases. Clin Spine Surg 29:86-9.
[2] Kim SI, Ha KY, Lee JW, Kim YH (2017) Prevalence and related clinical factors of thoracic ossification of the ligamentum flavum-a computed tomography-based cross-sectional study. Spine J pii: S1529-9430(17)30914-2.
[3] Mori K, Kasahara T, Mimura T, Nishizawa K, Murakami Y, Matsusue Y, Imai S (2013) Prevalence, distribution, and morphology of thoracic ossification of the yellow ligament in Japanese: results of CT-based cross-sectional study. Spine 38: E1216-22.
[4] Guo JJ, Luk KD, Karppinen J, Yang H, Cheung KM (2010) Prevalence, distribution, and morphology of ossification of the ligamentum flavum: a population study of one thousand seven hundred thirty-six magnetic resonance imaging scans. Spine 35: 51-6.
[5]Tanaka Y, Sato T, Aizawa T. Surgery for Ossification of the Ligamentum Flavum[M]// OPLL. Springer Japan, 2006:265-269.
[6] Li Z, Ren D, Zhao Y, Hou S, Li L, Yu S, Hou T (2016) Clinical characteristics and surgical outcome of thoracic myelopathy caused by ossification of the ligamentum flavum: a retrospective analysis of 85 cases. Spinal Cord 54:188-96. [7] Wang H, Wei F, Long H, Han G, Sribastav SS, Li Z, Huang Y, Zhu R, Liang C (2017) Surgical outcome of thoracic myelopathy caused by ossification of ligamentum flavum. J Clin Neurosci 45:83-88.
[8] 17. Jia LS, Chen XS, Zhou SY, Shao J, Zhu W (2010) En bloc resection of lamina and ossified ligamentum flavum in the treatment of thoracic ossification of the ligamentum flavum. Neurosurgery 66:1181-6.
[9] Mohindra S, Gupta R, Chhabra R, Gupta SK (2011) Compressive myelopathy due to ossified yellow ligament among South Asians: analysis of surgical outcome. Acta Neurochir (Wien). 2011 153:581-7.
[10]Sun J, Shi J, Xu X, et al. Anterior controllable antidisplacement and fusion surgery for the treatment of multilevel severe ossification of the posterior longitudinal ligament with myelopathy: preliminary clinical results of a novel technique.[J]. European Spine Journal, 2017(6):1-10.
[11] Miyakoshi N, Shimada Y, Suzuki T, Hongo M, Kasukawa Y, Okada K, Itoi E (2003) Factors related to long-term outcome after decompressive surgery for ossification of the ligamentum flavum of the thoracic spine. J Neurosurg 99: 251-6.
[12] Wang W, Kong L, Zhao H, Dong R, Li J, Jia Z, Ji N, Deng S, Sun Z, Zhou J (2007) Thoracic ossification of ligamentum flavum caused by skeletal fluorosis. Eur Spine J 16:1119-28.
[13] Gao R, Yuan W, Yang L, Shi G, Jia L (2013) Clinical features and surgical outcomes of patients with thoracic myelopathy caused by multilevel ossification of the ligamentum flavum. Spine J 13:1032-8.
[14] Young WF, Baron E (2001) Acute neurologic deterioration after surgical treatment for thoracic spinal stenosis. J Clin Neurosci 8:129-32.
[15] Wang H, Ma L, Xue R, Yang D, Wang T, Wang Y, Yang S, Ding W (2016) The incidence and risk factors of postoperative neurological deterioration after posterior decompression with or without instrumented fusion for thoracic myelopathy. Medicine (Baltimore) 95: e5519.
[16] Ito Z, Matsuyama Y, Ando M, Kawabata S, Kanchiku T, Kida K, Fujiwara Y, Yamada K, Yamamoto N, Kobayashi S, Saito T, Wada K, Tadokoro N, Takahashi M, Satomi K, Shinomiya K, Tani T (2016) Postoperative Paralysis From Thoracic Ossification of Posterior Longitudinal Ligament Surgery Risk Factor of Neurologic Injury: Nationwide Multiinstitution Survey. Spine (Phila Pa 1976) 41: E1159-E1163.




 京公网安备11010502051256号
京公网安备11010502051256号